Teman teman sudah tahu tentang difusi kan, Nah Osmosis adalah salah satu bentuk difusi tapi yang menyebar bukan lagi zat terlarut melainkan pelarutnya. Kita ketahui difusi adalah proses atau peristiwa bergeraknya zat dari konsentrasi tinggi menuju konsentrasi rendah.
Pengertian Osmosis
Osmosis juga merupakan perpindahan zat, walaupun ada perbedaan. Osmosis adalah proses perpindahan zat pelarut dari konsentrasi terlarut rendah ke konsentrasi terlarut tinggi. Sudah Jelas bahwa difusi sangat berbeda dengan osmosis jika dilihat dari pengertian osmosis ini.
Osmosis pada akhirnya akan membuat konsentrasi zat terlarut kedua bagian sama. Kenapa sama. Hal itu karena pelarut dari konsentrasi rendah akan pindah ke konsentrasi terlarut tinggi dan membuat perbandingan antara zat pelarut dan terlarut keduanya setara.
Osmosis sendiri sangatlah penting bagi makhluk hidup khususnya pada membran sel makhluk hidup. Peristiwa osmosis ini memungkinkan bagi molekul molekul kecil yang berperan penting dalam metabolisme sel dapat masuk ke dalam sitoplasma sel.
Osmosis adalah salah satu jenis transpor pasif pada sel. Osmosis Disebut sebagai transport pasif karena tidak menggunakan ATP atau energi kimiawi sel dalam melaksanakan prosesnya. Murni karena adanya perbedaan konsentrasi zat terlarut dan bukan jenisnya.
Pada materi osmosis ini kita akan mempelajari beberapa bagian, mulai dari:
- Sejarah Osmosis
- Mekanisme Osmosis
- Faktor yang mempengaruhi Osmosis
- Contoh Osmosis
- Manfaat dan Fungsi Osmosis
Sejarah Osmosis
Sejarah penemuan osmosis diketahui telah sering digunakan pada masa Mesir kuno, pada saat pembangunan Piramida di Mesir. Orang yang pertama menuliskan dan mengamati tentang osmosis adalah Jean-Antoine Nollet pada tahun 1748.
Osmosis sendiri merupakan turunan dari kata “Endosmose” dan “Exosmose” yang digunakan oleh Rene Joachim Henri Dutrochet, seorang fisikawan Prancis, yang hidup tahun 1776-1847.
Pada tahun 1867, peneliti bernama Moritz Traube menemukan sebuah alat untuk mengukur aliran osmosis. Alat ini menggunakan membran yang sangat selektif yang dapat membuktikan adanya osmosis dan mengukur aliran omosis itu sendiri.
Mekanisme Osmosis
Pengertian osmosis adalah transpor molekul pelarut melalui membran semipermeabel dari konsentrasi terlarut rendah menuju konsentrasi terlarut tinggi. Dapat juga kita katakan bahwa osmosis adalah perpindahan molekul air dari larutan hipotonik menuju larutan hipertonik yang pada akhirnya membentuk larutan isotonik.
Osmosis memang dikenali terjadi pada pelarut seperti air, walaupun begitu peristiwa osmosis tidak hanya terjadi pada air, dapat juga terjadi pada cairan pelarut lainnya dan bahkan gas.
Mekanisme osmosis sederhananya dapat kita amati ketika kita memasukkan sel ke dalam air. Molekul air dapat bergerak ke dalam ataupun keluar tergantung konsentrasi zat terlarur.
Sebagai contoh osmosis, ketika kita meletakkan sel tumbuhan ke dalam air garam (air laut), molekul air akan bergerak ke luar sel. Hal ini karena zat terlarut yang ada pada air laut bersifat hipertonik dibandingkan sel. Sebaliknya, ketika sel di air tawar (freshwater) maka molekul air akan masuk ke dalam sel. Hal tersebut karena air dalam air tawar bersifat hipotonik dibandingkan hipertonik.
Osmosis sendiri bersifat koligatif yang artinya merupakan gabungan konsentrasi, bukan hanya konsentrasi dari satu jenis zat.
Osmosis pada Sel Tumbuhan
Dalam mekanisme kerja osmosis, diketahui bahwa tekanan osmosis sangatlah penting bagi sel khususnya sel tumbuhan. Ketika sel tumbuhan diletakkan di dalam larutan yang hipertonik (berkonsentrasi larutan tinggi) maka sel tumbuhan akan mengerut. Semakin mengerutnya sel dapat membuat sel tersebut mengalami plasmolisis atau pecah.
Plasmolisis ini terjadi karena membran sel terpisah dengan dinding sel akibat kurangnya tekanan air dalam sel atau disebut tekanan turgor yang mempertahankan bentuk sel tumbuhan.
Selanjutnya ketika sel tumbuhan diletakkan ke dalam larutan hipotonik dibandingkan sitoplasma sel tumbuhan, maka akan terjadi osmosis yang membuat sel kemasukan air dan mengembang sehingga menjadi turgid.
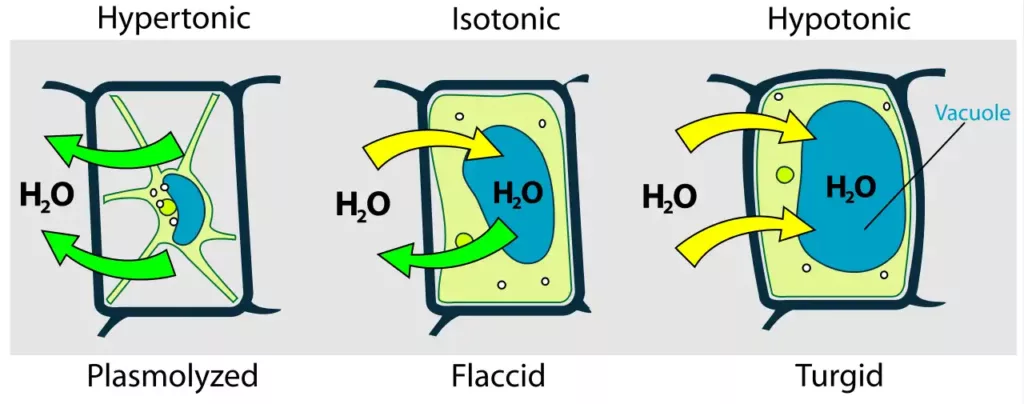
Ketika sel tumbuhan berada pada larutan isotonik, osmosis tidak berhenti, melainkan terjadi pertukaran air yang setimbang antara keluar dan masuk sel sehingga diperoleh net atau hasil bersih sama dengan nol.
Osmosis Pada Sel Hewan
Mekanisme osmosis pada sel darah merah pun mirip seperti ini. Perbedaannya tentu saja pada kehadiran dinding sel yang menjaga sel tumbuhan untuk sulit pecah.
Osmosis sel darah merah ketika berada pada larutan hipertonik maka air dari dalam sel darah merah akan keluar. Hal ini membuat sel darah merah mengecil dan akhirnya rusak.
Sebaliknya, Osmosis sel darah ketika berada pada larutan hipotonik membuat sel darah merah kemasukan air dan mengembang. Hal ini dapat membuat sel darah merah pecah.
Selanjutnya pada larutan isotonik, mekanisme osmosis terjadi keseimbangan antara air yang keluar dan air yang masuk.
Faktor yang mempengaruhi osmosis
Berikut adalah beberapa faktor yang mempengaruhi osmosis:
- Konsentrasi zat. Semakin tinggi perbedaan konsentrasi zat terlarut dalam kedua larutan yang dipisahkan oleh membran semipermeabel maka kecepatan osmosis akan semakin meningkat. Semakin mendekati equilibirium atau membentuk larutan isotonik, maka kecepatannya akan sangat lambat.
- Suhu, suhu sangat mempengaruhi pergerakan molekul. Dalam batas yang dimunkinkan (normal), semakin tinggi suhu, maka kecepatan osmosis juga semakin tinggi. Ketika suhu sangat rendah, hingga cairan membeku, osmosis dapat berhenti.
- Tekanan Osmosis, tekanan ini diperoleh dengan menambahkan tekanan pada larutan hipertonik sehingga menambahkan kecepatan osmosis yang terjadi. Hal ini sering dilakukan pada pemurnian air, desalinisasi dan semacamnya.
- Ukuran molekul pelarut, semakin besar molekul pelarut maka akan semakin sulit untuk molekul tersebut melintasi membran semipermeabel
- Luas membran, semakin luas membran maka akan semakin cepat perpindahan molekul airnya.
Contoh Osmosis
Ada banyak contoh osmosis yang bisa kita temukan disekitar kita. Bahkan dapat kita katakan bahwa semua makhluk hidup di muka bumi ini mengalami osmosis.
Berikut beberapa contoh peristiwa osmosis yang ada disekitar kita.
- Sel darah yang masuk ke dalam air garam akan mengerut, ketika masuk ke dalam air suling (akuades) akan mengembang.
- Kentang yang direndam dalam larutan garam akan mengerut karena air dalam sel kentang akan keluar menuju larutan hipertonik.
- Melepaskan lintah (atau membunuh lintah) yang menghisap dengan menaburkan garam ataupun merendam dalam larutan garam.
- Peristiwa masuknya air ke dalam akar terjadi karena peristiwa osmosis.
- Peristiwa buka tutup stomata juga karena adanya osmosis
Manfaat dan Fungsi Osmosis
Berikut adalah beberapa manfaat osmosis dan fungsi osmosis yaitu:
- Fungsi osmosis bagi tumbuhan adalah pada peristiwa masuknya air ke dalam akar sehingga air tersebut dapat dihantarkan ke seluruh bagian sel tumbuhan khususnya yang mengalami fotosintesis.
- Fungsi osmosis dalam penyaringan air
- Berperan penting dalam pembentukan air minum menggunakan air garam (desalinsasi)
- Manfaat osmosis bagi kerja tubuh manusia khususnya dalam aktivitas ekskresi pada ginjal.
- Cuci darah atau dialisis juga menggunakan prinsis osmosis.
Sekian artikel tentang osmosis ini. Semoga bermanfaat dan berguna bagi teman teman semua.